Les tumeurs du cerveau
Le terme de tumeurs cérébrales englobe généralement les tumeurs du cerveau et de ses enveloppes, les méninges. Elles peuvent se manifester par des maux de tête, des nausées, des vomissements, une vision double ou d’autres signes d’hypertension intracrânienne. Si elles irritent la surface du cerveau ou cortex, elles peuvent causer des crises d’épilepsie.
Enfin, si elles irritent ou détruisent des zones fonctionnelles importantes du cerveau, elles peuvent s’accompagner de perte de force (hémiplégie) ou de troubles de la parole pouvant aller jusqu’à l’aphasie.
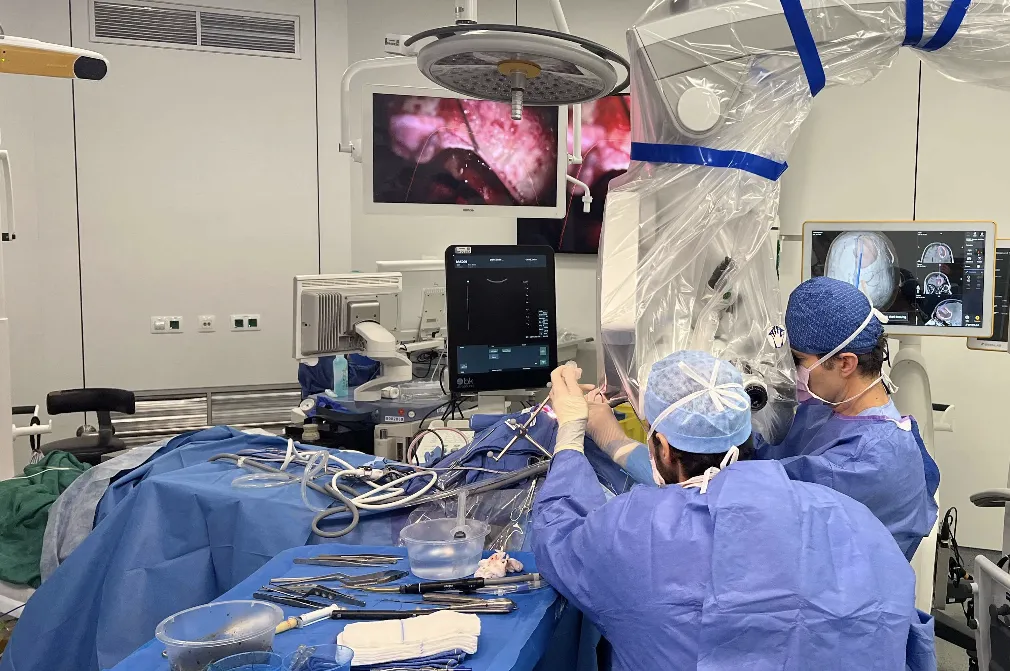
Le traitement chirurgical de ces tumeurs fait en général appel à une technique très sophistiquée : chirurgie assistée par ordinateur, neuronavigation, chirurgie en conditions stéréotaxiques ou endoscopique, résection par aspirateur à ultrasons, microscope opératoire, micro-instruments, fraises à haute vitesse, embolisation préopératoire. Bien que ces techniques permettent d’obtenir des résultats en progrès constant tant du point de vue de la survie des patients que de la qualité de vie, les tumeurs cérébrales restent une pathologie redoutable tant sur le plan fonctionnel que vital.
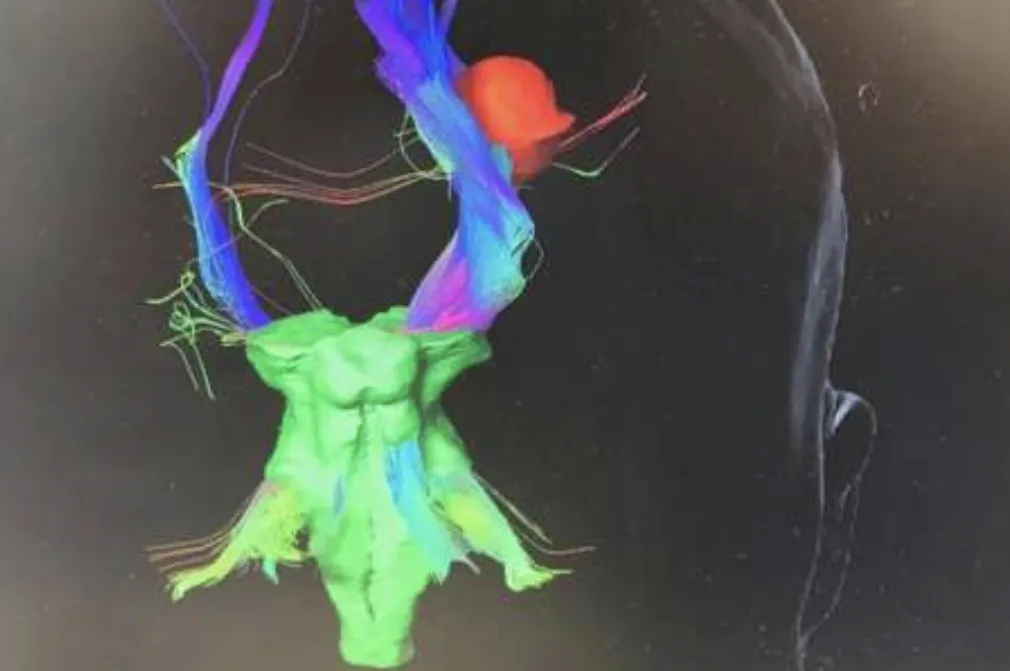
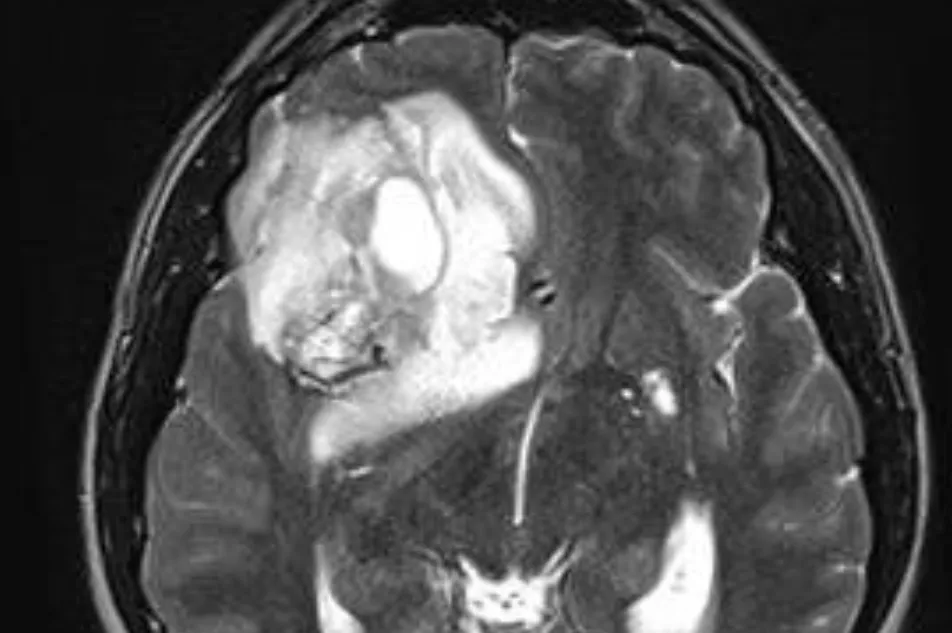
Les tumeurs gliales ou gliomes sont issues du cerveau lui-même, formées à partir des cellules gliales du cerveau. On distingue des gliomes bénins (astrocytomes, oligodendrogliomes, etc..) et les gliomes malins (astrocytome anaplasique, glioblastome) :
Les gliomes bénins sont souvent infiltrants, ne peuvent pas toujours être guéris par la chirurgie seule et vu la possibilité de récidive, doivent être suivis régulièrement même après une intervention. Il n’est pas toujours nécessaire de les opérer de manière agressive et parfois une simple biopsie est suffisante. Leur pronostic est en général assez favorable.
Les gliomes malins sont nettement plus agressifs et leur pronostic est nettement plus réservé. L’astrocytome anaplasique et le glioblastome nécessitent soit une biopsie, soit le plus souvent une résection chirurgicale selon l’endroit où ils sont placés, puis souvent une chimiothérapie et/ou une radiothérapie. Ces tumeurs ont tendance à récidiver rapidement et même après seulement quelques mois pour le glioblastome.
Les métastases cérébrales sont des tumeurs malignes issues d’une tumeur cancéreuse située ailleurs dans l’organisme (cancers du rein, du sein, du poumon, du côlon, mélanome ou autres). Lorsqu’elles sont uniques et symptomatiques, elles peuvent bénéficier d’un traitement agressif, soit par microchirurgie et radiothérapie, soit par Gamma Knife. Le pronostic de ce type de tumeur est très réservé et dépend surtout de la possibilité de contrôle de la maladie cancéreuse à l’origine de la métastase.
Les tumeurs gliales ou gliomes sont issues du cerveau lui-même, formées à partir des cellules gliales du cerveau. On distingue des gliomes bénins (astrocytomes, oligodendrogliomes, etc..) et les gliomes malins (astrocytome anaplasique, glioblastome)
Les gliomes bénins sont souvent infiltrants, ne peuvent pas toujours être guéris par la chirurgie seule et vu la possibilité de récidive, doivent être suivis régulièrement même après une intervention. Il n’est pas toujours nécessaire de les opérer de manière agressive et parfois une simple biopsie est suffisante. Leur pronostic est en général assez favorable.
Les gliomes malins sont nettement plus agressifs et leur pronostic est nettement plus réservé. L’astrocytome anaplasique et le glioblastome nécessitent soit une biopsie, soit le plus souvent résection chirurgical selon l’endroit où il est placé, puis souvent une chimiothérapie et/ou une radiothérapie. Ces tumeurs ont tendance à récidiver rapidement et même après seulement quelques mois pour le glioblastome.
Les adénomes hypophysaires sont majoritairement des tumeurs bégnines qui se développent à partir de la glande hypophysaire.
On peut les catégoriser par leur activité et par leur volume. En effet, ceux-ci peuvent secréter de manière excessive des hormones hypophysaires ou peuvent, par leur volume, comprimer les structures fonctionnelles et, en particulier, le nerf optique et le chiasma.
Les adénomes secrétants sont habituellement découverts de manière plus précoce et sont le plus souvent catégorisés comme des micro-adénomes. Leur traitement est, dans un premier temps, le plus souvent médicamenteux et, en cas d’échappement du traitement médical, peut être chirurgical. Il nécessite dès lors une étroite collaboration entre les endocrinologues et les neurochirurgiens.
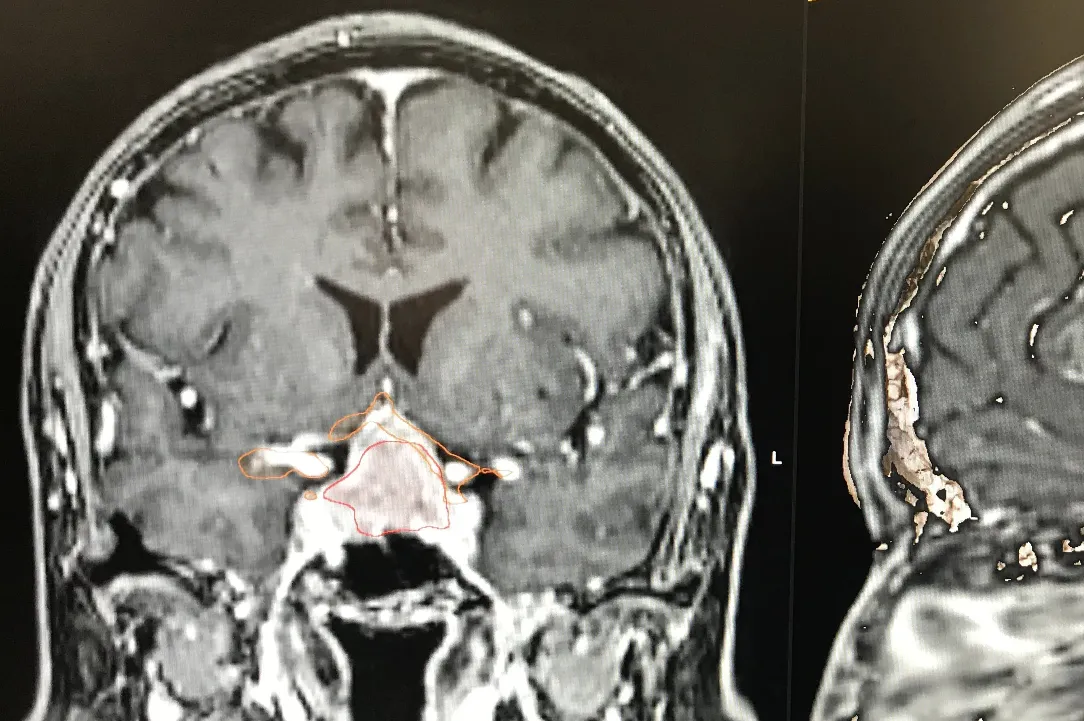
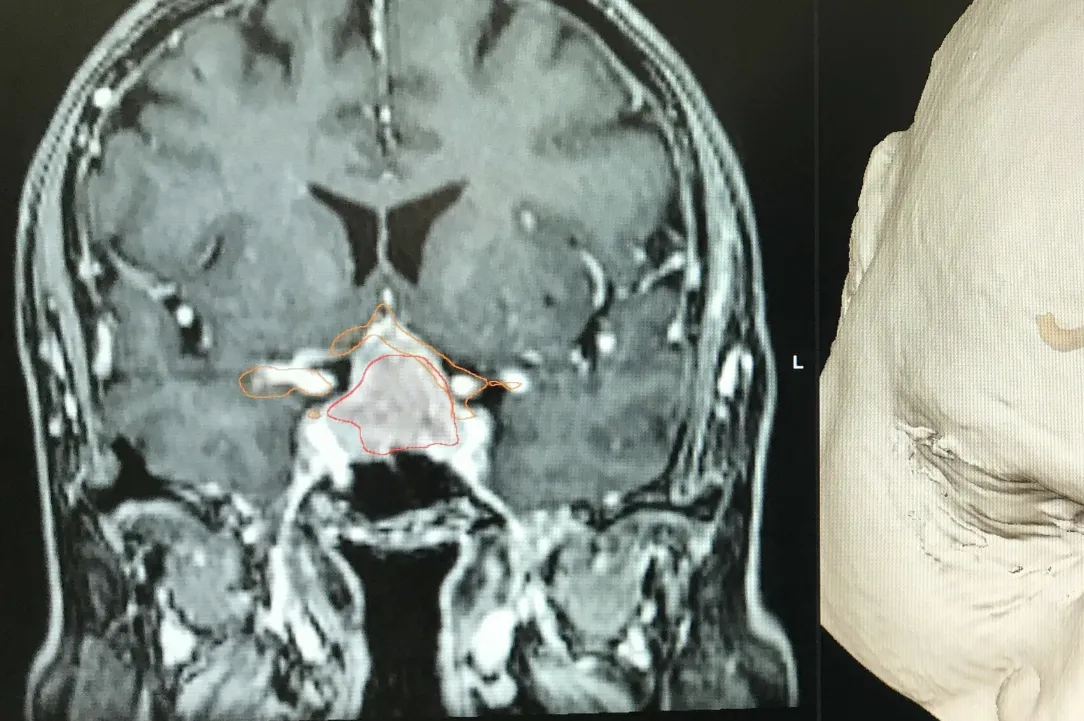
Les adénomes non-secrétants sont souvent découverts soit de manière fortuite lors d’une imagerie cérébrale, soit en lien avec leur volume excessif. On parle alors de macroadénomes qui sont responsables de troubles le plus souvent visuels par compression du nerf optique et ou du chiasma. Leur traitement est chirurgical s’ils sont symptomatiques. L’acte chirurgical consiste à l’exérèse de la tumeur via les cavités nasales et le sinus sphénoïdale (voie transnasale, transphénoïdale). L’abord peut se faire sous endoscope ou microscope. La tendance actuelle est d’utiliser la voie endoscopique en étroite collaboration avec l’équipe d’ORL. Dans certaines situations, un traitement combinant l’exérèse chirurgicale et un traitement par radiochirurgie peut être discuté en concertation oncologique multidisciplinaire. Vous retrouverez au sein de notre service de Neurochirurgie du CHIREC, l’ensemble de ces collaborations possibles.
Parmi les autres tumeurs, citons :
Les tumeurs de la base du crâne : schwannomes vestibulaires ou neurinomes de l’acoustique, chordomes.
Les tumeurs du système ventriculaire : épendymomes, les subépendymomes, les papillomes des plexus choroïdes.
Toutes ces tumeurs s’accompagnent d’une symptomatologie particulière et requièrent un traitement et une prise en charge très spécifique.
La névralgie du nerf trijumeau
Au sein de notre service de neurochirurgie, nous privilégions la décompression du nerf trijumeau. Au sein de l’hôpital Delta, nous avons acquis un système de traitement percutané navigué permettant de faire une compression du ganglion de gassser par ballonnet. La névralgie du trijumeau est une douleur faciale paroxystique lancinante, sévère, due à un trouble du 5e nerf crânien. Le diagnostic est clinique. Le traitement comprend habituellement la carbamazépine ou la gabapentine; parfois, une intervention chirurgicale est nécessaire. La névralgie du trijumeau touche principalement les adultes, en particulier les personnes âgées. Il est plus fréquent chez la femme. La névralgie du trijumeau est généralement provoquée par :
- Compression du nerf trijumeau à sa racine par une boucle aberrante d'une artère intracrânienne (p. ex., artère cérébelleuse antérieure inférieure, artère basilaire ectasique)
- Moins souvent, par une boucle veineuse qui comprime le 5e nerf crânien (nerf trijumeau) à son entrée dans le tronc cérébral
Une cause moins fréquente est la compression par une tumeur, une malformation artérioveineuse, un anévrisme, et, parfois, une plaque de sclérose en plaques dans la zone d'entrée des racines (en général des patients jeunes), mais ces causes se distinguent par la présence d'une hypoesthésie et d'autres déficits. D'autres troubles qui causent des symptômes semblables (p. ex., sclérose en plaques) sont parfois considérés comme une névralgie du trijumeau et parfois non. Reconnaître la cause sous- jacente est important. Le mécanisme est mal connu. Une théorie suggère que la compression du nerf entraîne une démyélinisation locale, ce qui peut entraîner la genèse d'impulsions ectopiques (transmission éphaptique) et/ou une désinhibition des voies de la douleur centrale impliquant le noyau spinal du trijumeau.
La douleur de la névralgie du trijumeau survient dans le territoire d'une ou plusieurs branches sensitives du nerf trijumeau, le plus souvent la branche maxillaire. La douleur est paroxystique, dure de quelques secondes à 2 min, mais les accès peuvent rapidement récidiver, avec une fréquence pouvant aller jusqu'à 100 fois/jour. Elle est lancinante, intense et parfois invalidante. La douleur peut souvent être déclenchée en touchant une zone gâchette du visage (p. ex., mastication, brossage des dents ou en souriant). Dormir sur le côté atteint est souvent intolérable. Habituellement, un seul côté du visage est affecté.
Les symptômes de la névralgie du trijumeau sont souvent pathognomoniques. Ainsi, certains autres troubles qui causent des douleurs faciales peuvent être différenciés cliniquement :
- L'hémicrânie paroxystique chronique (syndrome de Sjaastad) se distingue par des crises douloureuses plus longues (5 à 8 min) et son amélioration spectaculaire sous l'effet de l'indométhacine.
- La douleur post-zostérienne est différenciée par son caractère persistant (sans paroxysmes), un antécédent récent d'éruption caractéristique, la présence de cicatrices et à sa prédilection pour la branche ophtalmique.
- La migraine, qui peut entraîner des douleurs faciales atypiques, est différenciée par une douleur plus prolongée et souvent pulsatile.
- La sinusite et la douleur odontogène qui peuvent habituellement être différenciées par les signes associés (p. ex., écoulement nasal, fièvre, céphalées positionnelles, sensibilité des dents).
- Habituellement, antiépileptiques
La névralgie du trijumeau est traitée par la carbamazépine 200 mg par voie orale 3 ou 4 fois/jour, ce qui est habituellement efficace pendant de longues périodes; elle est débutée à 100 mg par voie orale 2 fois/jour, en augmentant la dose de 100 à 200 mg/jour jusqu'à ce que la douleur soit contrôlée (dose quotidienne maximale 1200 mg). Si la carbamazépine est inefficace ou a des effets indésirables, un des médicaments oraux suivants peut être essayé : le bloc nerveux périphérique procure un soulagement temporaire. La toxine botulique peut être injectée entre l'épiderme et le derme aux points de déclenchement où la douleur est ressentie ou le long du trajet des branches nerveuses impliquées. Ce traitement peut être bénéfique, mais les données sont limitées. Si la douleur reste intense malgré ces mesures, le traitement par destruction neuronale peut être envisagé ; l'efficacité peut cependant être temporaire et l'amélioration peut être suivie d'une douleur persistante encore plus intense que les épisodes préexistants.
La chirurgie qui soulage la douleur peut entraîner un engourdissement facial. Un engourdissement douloureux (anesthésie douloureuse) peut également en résulter; elle survient chez 4% des patients après rhizotomie. Lors d'une craniectomie de la fosse postérieure, un petit tampon peut être placé dans le but de séparer la boucle vasculaire pulsatile de la racine du trijumeau (appelée décompression microvasculaire, ou procédure de Jannetta). Dans la radiochirurgie au gamma-knife, le rayonnement gamma est focalisé sur le nerf trijumeau proximal au moment où il sort du tronc cérébral; cette procédure interrompt les signaux de douleur vers le cerveau. Des lésions électrolytiques thermocoagulation ou chimiques ou une compression par ballonnet gonflable du ganglion du trijumeau (de Gasser) peuvent être pratiquées par voie percutanée, par l'intermédiaire d'une sonde introduite par stéréotaxie. Parfois, les fibres du trijumeau sont sectionnées entre le ganglion de Gasser et le tronc cérébral. Parfois aussi, pour soulager une douleur rebelle, une destruction du trijumeau peut être proposée en dernier recours.
Les hémorragies cérébrales
Les hémorragies cérébrales peuvent être la conséquence de plusieurs types de situations :
- Hémorragie sous arachnoïdienne (HSA) sur rupture d’anévrisme.
- Hémorragie sur rupture de malformation artério veineuse (MAV).
- Hémorragie sur angiome caverneux
- Hémorragie d’origine traumatique.
- Hémorragie « spontanée » sur hypertension artérielle (HTA), artériosclérose, amyloïdose, etc…
Un anévrisme cérébral est une dilatation anormale d’une artère du cerveau, dont la rupture peut avoir des conséquences dramatiques conduisant à des séquelles neurologiques majeures ou à la mort dans plus de la moitié des cas.
Un anévrisme cérébral ou intracrânien est une hernie (anévrisme sacculaire), ou une dilatation (anévrisme fusiforme) de la paroi artérielle. Ils se rencontrent généralement entre 35 et 60 ans et touchent environs 1% de la population.
Les anévrismes peuvent être découverts par hasard (lors d’un scanner, d’une IRM). Cependant, ils sont généralement révélés soit par les signes neurologiques liés à la compression des structures avoisinantes, soit lors de leur rupture avec Hémorragie Sous-Arachnoïdienne (HSA) qui peut entraîner des lésions cérébrales et même le décès.
Le but principal du traitement d’un anévrisme est d’empêcher l’hémorragie ou de l’arrêter en cas de rupture. Deux options thérapeutiques existent actuellement et sont discutées pour chaque cas à DELTA. L’option chirurgicale consiste par la mise en place d’un clip sur le collet de l’anévrisme alors que le traitement endovasculaire consiste à l’occlusion de l’anévrysme par la mise en place spires métalliques (les coils) dans la malformation. Le Traitement Endovasculaire est réalisé sous anesthésie générale et nécessite l’insertion d’un micro-cathéter au pli inguinal du malade, cathéter qui est amené sous contrôle fluoroscopique dans les artères cervicales, puis cérébrales jusqu’au sein du sac anévrismal. Plusieurs coils sont alors déployés dans l’anévrysme jusqu’à l’exclusion du flux sanguin par un maillage serré, engendrant la thrombose de l’anévrisme. Comme les coils sont radiopaques, le neuroradiologue contrôle leur positionnement correct dans l’anévrisme sous contrôle scopique.
Parfois, le coiling se fait aussi à l’aide de la mise en place d’un stent et, plus récemment, par la mise en place d’une prothèse (WED).
Chacune de ces méthodes a ses avantages et inconvénients. Nous avons, à DELTA, l’expérience de ces 2 techniques et nous nous engageons à choisir le traitement optimal pour nos patients.

Les pathologies lombaires & cervicales
Une hernie discale est le déplacement d’un morceau du noyau pulpeux du disque à travers une déchirure de l’anneau fibreux. La hernie s’isole alors du reste du disque, sort dans le canal rachidien où elle peut comprimer les racines nerveuses. Cette situation est une des meilleures indications chirurgicales, et peut ne pas répondre favorablement aux traitements conservateurs, aux manipulations ou à la chimonucléolyse.
La hernie est souvent précédée d’un ou plusieurs épisodes de lombalgies, mais lorsque la hernie commence à comprimer une racine nerveuse apparaît une « sciatique », douleur partant du bas du dos et irradiant dans la jambe selon un trajet caractéristique dépendant du nerf comprimé. Elle peut s’accompagner de perte de force dans les jambes ou de modifications des réflexes rotuliens ou achilléens.
Un scanner ou une résonance magnétique de la colonne lombaire est en général réalisé, permettant de montrer la taille de la hernie, l’état des autres disques et le calibre du canal lombaire.
Le traitement de la hernie discale est en général conservateur en première intention, c’est-à-dire non chirurgical, composé d’une mise au repos de la colonne, parfois aidée d’antalgiques, de myorelaxants ou d’anti-inflammatoires oraux, d’une ou plusieurs infiltrations péridurales ou de kinésithérapie. En cas d’inefficacité de ces traitements, de persistance des douleurs et de persistance ou accentuation d’un déficit moteur, une intervention chirurgicale doit être envisagée.
L’intervention consiste en général en une micro-discectomie, permettant d’ôter le fragment exclu. La sciatique disparaît en général rapidement, mais l’inconfort dans la région lombaire peut persister durant plusieurs semaines.
En général de 80 à 85 % des patients sont soulagés après l’intervention chirurgicale et peuvent reprendre leurs activités et leur travail. Le risque de récidive au même niveau est d’environ 5% et est plus élevé en cas d’excès pondéral ou de travail lourd. Même après chirurgie et sans récidive, 5% des patients continuent à présenter des douleurs chroniques pouvant limiter ou empêcher un retour au travail ou à une vie normale, sans que ce soit nécessairement une conséquence directe de l’intervention chirurgicale.
Nous conseillons vivement aux patients présentant une hernie discale lombaire, opérée ou non, de suivre les cours de l’Ecole du Dos à l’Hôpital DELTA ou autre centre agréé ou encore par un kinésithérapeute compétent. Le patient sera éduqué à renforcer la musculature abdominale et paravertébrale et à respecter les bons gestes de manière à optimaliser le traitement neurochirurgical.
Depuis plusieurs années, le “golden standard” du traitement de la hernie discale cervicale était devenu la discectomie par abord antérieur suivie dans la plupart des cas par une arthrodèse avec mise en place de cage intersomatique en titane ou en PEEK. Les résultats de cette intervention étaient très satisfaisants à court et moyen terme, mais une usure prématurée des disques voisins sus et sous-jacents à l’arthrodèse a été remarquée.
La recherche chirurgicale s’est donc appliquée à trouver une solution qui permette non seulement d’ôter le disque générateur de douleur et de restaurer la hauteur du disque, mais aussi de restaurer l’équilibre vertébral, de restaurer la mobilité et de protéger les niveaux voisins d’une usure prématurée. Dans cette optique ont été développées les prothèses discales cervicales.
L’intérêt majeur de ces prothèses cervicales réside donc dans le maintien de la mobilité et la protection des niveaux voisins. L’intervention est réalisée sous microscope, consiste en l’exérèse du disque et de la hernie discale comprimant des structures nerveuses, puis en la mise en place de l’implant dans l’espace intervertébral.
Ces implants se composent de deux plateaux en titane couverts d’un coating en plasmapore permettant une intégration osseuse aux vertèbres adjacentes, et d’une interface en polyéthylène (prothèse Baguera –C, Spineart) jouant le rôle d’articulation entre les deux vertèbres.
Le bilan préopératoire reste classique, comportant radiographies simples, CT scan et/ou IRM cervicale et éventuellement discographie ou densitométrie osseuse.
Pour les indications chirurgicales de ce type d’intervention, nous suivons les « guidelines » de la BNSS (Belgian Neurosurgical Spine Society) et envisageons en général la pose d’une prothèse discale cervicale dans les cas de hernie discale “molle” chez un patient de moins de 55 ans, présentant une hauteur discale encore préservée, avec peu d’arthrose facettaire ou discale, et dans les cas de décompensation discale au voisinage d’une arthrodèse préalable ou d’une fusion congénitale. La prothèse discale n’est bien entendu pas indiquée en cas d’ostéoporose, de sténose du canal rachidien cervical, d’instabilité vertébrale (spondylolisthésis), de tumeur ou de fracture.
Actuellement, une seule prothèse est remboursée par l’INAMI (MOBI C). Dans notre service, nous suivons de près les résultats des prothèses cervicales, afin de recueillir les données qui permettront de développer des prothèses de plus en plus performantes et de connaître le devenir réel du niveau adjacent à long terme, la technique d’implantation idéale ou l’usure de l’implant. Les patients porteurs d’une prothèse Baguera C sont d’ailleurs suivis plus spécialement dans le cadre d’une étude clinique entamée en 2010.
Nous avons à présent près de 20 ans d’expérience dans la mise en place des prothèses discales cervicales, qui sont devenues une intervention à part entière, traitement original, anatomique et physiologique de la maladie discale cervicale.
Un canal lombaire étroit est un rétrécissement du canal rachidien causant une compression des nerfs de la queue de cheval qui commandent les jambes. C’est en général une pathologie d’origine dégénérative survenant chez le sujet de plus de 60 ans.
Il se manifeste par une douleur, dans le bas du dos ou dans les fesses, irradiée dans les jambes, accentuées par la marche, qui devient de plus en plus limitée. On parle alors d’une réduction du périmètre de marche. La douleur est améliorée par le repos en position assise ou couchée, ou par la flexion en avant du tronc. Dans les cas extrêmes, les patients peuvent perdre la marche ou le contrôle de la vessie ou des selles.
Le bilan radiologique comporte en général des radiographies simples ou un scanner de la colonne lombaire, mais la résonance magnétique est l’examen le plus performant permettant de définir l’importance et la longueur du rétrécissement. Une myélographie ou un myélo-CT est parfois demandé lorsqu’une résonance n’est pas réalisable.
Les traitements du canal lombaire étroit peuvent être conservateurs ou chirurgicaux :
- Le traitement conservateur est basé sur la prise d’anti-inflammatoires, de kinésithérapie ou d’infiltrations péridurales. Son efficacité est en général temporaire.
- Pour une amélioration plus durable, le traitement de choix est chirurgical, permettant une amélioration des douleurs dans 74% des cas. L’intervention chirurgicale est recommandée chez les patients présentant un état de santé relativement bon, lorsque la douleur rend la marche ou la position debout impossible ou difficilement supportable malgré la prise de médications, et surtout lorsque les patients présentent des déficits neurologiques.
Plusieurs types d’intervention peuvent être proposés, selon la sévérité du rétrécissement. Nous privilégions la décompression canalaire par voie minimalement invasive et microchirurgicale. Très rarement, une arthrodèse est proposée au patient.
Il est important de discuter des risques de l’intervention, de l’influence des facteurs neurologiques et généraux sur la faisabilité de l’opération, des techniques utilisées, ainsi que des résultats à attendre de l’intervention.
Une arthrodèse lombaire consiste en une fixation l’une à l’autre de plusieurs vertèbres voisines au moyen de matériel d’ostéosynthèse, de manière à obtenir une fusion vertébrale après mise en place de greffons osseux.
Plusieurs situations pathologiques peuvent nécessiter ce type d’intervention :
- Malformations vertébrales : spondilolyse, spondylolisthésis.
- Instabilité vertébrale post opératoire : glissement vertébral après laminectomie décompressive ou pour tumeur vertébrale.
- Instabilité vertébrale d’origine arthrosique.
- Fractures vertébrales instables ou déformantes.
- Failed back : douleurs lombaires chroniques post opératoires, résistantes aux traitements conservateurs.
- Scolioses
Plusieurs techniques opératoires peuvent être proposées, ainsi que plusieurs types de matériel. Les interventions les plus fréquentes sont :
- Arthrodèse par vis pédiculaires et fixation postérieure seule.
- Fusion lombaire par vis pédiculaire, fixation postérieure et mise en place de cages intervertébrales par voie postérieure (PLIF).
- Fusion lombaire par vis pédiculaire, fixation postérieure et mise en place de cages intervertébrales par voie antérieure (ALIF), ou latérale (TLIF).
- Fusion lombaire par voie latérale (XLIF)
De plus en plus souvent, les arthrodèses lombaires pourront être réalisées de manière minimalement invasive, par voie percutanée. Cette technique nouvelle a l’avantage de permettre la mise en place du matériel d’ostéosynthèse (vis et tiges métalliques) à travers la peau sous contrôle radioscopique. Les interventions sont réalisées plus rapidement, avec des pertes sanguines minimales et un risque d’infection réduit.
D’une manière générale, les interventions d’arthrodèse ne doivent pas être envisagées à la légère et ne sont certainement pas une solution pour les patients souffrant de lombalgies chroniques d’origine musculaire ou dégénérative. La préservation des structures musculaires entourant la colonne vertébrale est précieuse et permet au patient de récupérer et un retour à la vie normale plus rapide.
Nous utilisons, à Delta, l’association d’une scopie 3D robotisée (phéno de chez Siemens) et la navigation spinale (BrainLab) permettant une implantation précise du matériel (vis pédiculaire, cage intersomatique) sans recourir à une radiographie peropératoire minimisant dès lors la radiation, à la fois du patient et du personnel soignant. Lien vers « La combinaison d’un scanner robotisé (matériel de haute technologie)
Le traitement des fractures vertébrales ostéoporotiques
Les fractures vertébrales peuvent ainsi survenir, parfois même après un traumatisme minime, et occasionner des douleurs nécessitant une hospitalisation, une impotence fonctionnelle rendant parfois la marche impossible, éventuellement une compression de la moelle épinière ou des racines nerveuses, une déformation de la colonne et des difficultés respiratoires par perte d’amplitude de la cage thoracique. L’évolution peut alors se faire vers une spirale d’altération des fonctions et de la qualité de vie, avec un taux de mortalité augmenté de près de 30% par rapport à une population normale du même âge.
Le traitement classique de la fracture vertébrale ostéoporotique jusqu’à présent se composait de repos au lit, d’antalgiques et de corsets, et dans de rares cas, un traitement chirurgical à visée surtout décompressive. Ces traitements, contraignants, n’étaient pas toujours suivis, ni efficaces ou bien tolérés, d’où le développement nécessaire de nouvelles techniques.
La kyphoplastie est ainsi apparue dans l’arsenal thérapeutique disponible pour traiter les fractures vertébrales. Il s’agit d’une intervention visant à soulager la douleur en stabilisant la fracture, et à réduire la déformation rachidienne en restaurant le plus possible la hauteur vertébrale.
Elle consiste en la mise en place percutanée sous contrôle radioscopique de deux trocarts dans les pédicules de la vertèbre fracturée jusque dans le corps vertébral, d’y introduire un ballonnet qui une fois gonflé restaure la hauteur de la vertèbre.
On crée ainsi un espace dans lequel, une fois les ballonnets retirés, on pourra injecter sous faible pression du ciment à prise rapide qui permettra de stabiliser la fracture et de maintenir la correction de hauteur obtenue. L’intervention est réalisée sous anesthésie générale, mais est d’une durée limitée de l’ordre de 30 à 45 minutes par vertèbre.
La kyphoplastie fait l’objet d’un remboursement conditionné qui ne s’applique malheureusement qu’à un nombre restreint d’indications.
Elle n’est donc remboursée que dans les cas de fractures ostéoporotiques présentant une perte de hauteur suffisante, une densitométrie osseuse attestant d’une ostéoporose sévère (-2,5 DS), une IRM avec signes d’œdème intravertébral, et après un délai de 8 semaines après la fracture.
Elle est aussi remboursée pour les fractures consécutives à une métastase de myélome. Les fractures tombant en dehors de ces conditions peuvent toutefois souvent être d’excellentes indications à un traitement par kyphoplastie, mais le coût du matériel sera alors à la charge du patient.
Le traitement des fractures vertébrales est donc un domaine en évolution constante, offrant de nouvelles possibilités aux patients souffrant de cette condition.

